Chiều 12/8, đại diện Cục An toàn Thực phẩm, Bộ Y tế, cho hay cơ quan này chỉ cấp giấy phép tiếp nhận công bố sản phẩm cho Công ty Cổ phần Dược Phẩm Vinh Gia ngày 29/6.
“Từ đó đến nay, doanh nghiệp chưa gửi hồ sơ xin phép quảng cáo, cơ quan quản lý chưa duyệt nội dung nên các thông tin quảng cáo liên quan tới công dụng của sản phẩm (nếu có) đều là trái phép”, vị lãnh đạo này cho hay.
Quy định đặt tên sản phẩm
Sản phẩm thực phẩm chức năng Vipdervir-C có tên gọi gần giống với sản phẩm thuốc Vipdervir do Viện Hàn lâm khoa học và Công nghệ Việt Nam phối hợp với Công ty Cổ phần Dược phẩm Vinh Gia phối hợp nghiên cứu sản xuất.
Ngày 12/8, với việc hai tên sản phẩm gần như trùng khớp, lãnh đạo Viện Hàn lâm khoa học và Công nghệ Việt Nam đã yêu cầu Công ty Cổ phần Dược phẩm Vinh Gia đổi tên sản phẩm thực phẩm chức năng Vipdervir C để tránh gây hiểu lầm.
Viện này cũng khẳng định công ty đã vi phạm hợp đồng ký kết về nghiên cứu, sản xuất thuốc Vipdervir.
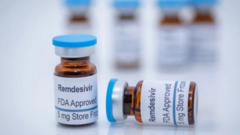
Sản phẩm Vipdervir-C được cấp phép trước thời điểm công bố thông tin thuốc điều trị COVID-19 Vipdervir hơn một tháng.
Không chỉ gần như giống nhau về tên gọi, nhãn mác 2 sản phẩm này cũng rất giống nhau là màu xanh đỏ chủ đạo.
Trước thời điểm công bố việc thử nghiệm lâm sàng thuốc Vipdervir, một số trang mạng đã xuất hiện các thông tin quảng cáo sản phẩm Vipdervir-C với nhiều công dụng. Trong đó, nổi bật nhất là công dụng giảm nguy cơ mắc bệnh do virus.
Một số chuyên gia y tế và dược sĩ cho rằng việc đặt tên gọi như vậy rất dễ gây hiểu lầm cho người dùng, nhất là thời điểm dịch COVID-19 đang bùng phát.
"Khi sản phẩm Vipdervir mới đang được chuyển qua giai đoạn lâm sàng mà truyền thông đăng tải rầm rộ, gọi là thuốc điều trị COVID-19 trong khi thị trường có sản phẩm tương tự, người dân rất dễ lầm tưởng và đổ xô đi mua", một chuyên gia nêu ý kiến.

Sản phẩm thuốc thử nghiệm Vipdervir. (Ảnh: VAST)
GS Nguyễn Bá Đức, nguyên Giám đốc Bệnh viện K, cũng cho hay các nước cấm đặt tên sản phẩm giống nhau. Tuy nhiên, Việt Nam chưa có quy định rõ ràng về vấn đề này.
Không cấp phép sản phẩm kháng virus
Liên quan việc quảng cáo sản phẩm thực phẩm chức năng mới đây, Cục An toàn Thực phẩm (Bộ Y tế) đã cảnh báo người dân về việc mua và sử dụng thực phẩm bảo vệ sức khỏe. Đặc biệt, cơ quan này khẳng định không cấp phép cho bất kỳ sản phẩm nào có công dụng kháng virus.
Theo cơ quan này, hiện nay, việc quảng cáo, bán thực phẩm bảo vệ sức khỏe qua hình thức online, gọi điện thoại cho người tiêu dùng rất phổ biến. Tuy nhiên, một số tổ chức, cá nhân lợi dụng hình thức bán hàng này để tư vấn thổi phồng công dụng sản phẩm sai quy định của pháp luật.
Nhiều trường hợp sản phẩm không có địa chỉ công ty, không có nơi bán hàng cố định, khách đặt hàng được người giao hàng đưa hàng và thu hộ tiền cho người bán, không có hóa đơn bán hàng. Do vậy, người tiêu dùng không rõ nguồn gốc sản phẩm để có thể truy cứu trách nhiệm khi sản phẩm không đúng như quảng cáo.
Cục An toàn Thực phẩm khẳng định thực phẩm bảo vệ sức khỏe không phải là thuốc, không có tác dụng thay thế thuốc chữa bệnh. Trong trường hợp có bệnh, người dân cần tới cơ sở y tế để khám và được điều trị kịp thời.
Điều 10 Thông tư 44/2014/TT-BYT quy định việc đăng ký thuốc do Bộ trưởng Y tế ban hành, việc đặt tên thuốc phải theo quy chuẩn như sau: Bộ Y tế khuyến khích các cơ sở đăng ký sử dụng tên thuốc theo tên chung quốc tế (INN). Trường hợp không đặt tên thuốc theo tên INN, cơ sở đăng ký thuốc có thể đặt tên thương mại cho thuốc. Tên thương mại của thuốc phải bảo đảm nguyên tắc sau đây: Không ghi quá tác dụng điều trị của thuốc. Không ghi sai tác dụng điều trị và tác dụng dược lý của thuốc. Không vi phạm thuần phong, mỹ tục, truyền thống của Việt Nam. Không gây xung đột với các đối tượng sở hữu trí tuệ của cá nhân, tổ chức khác đang được bảo hộ. Không trùng hoặc tương tự với tên thuốc đã được cấp số đăng ký của cơ sở khác. Không được đặt tên thuốc giống nhau nếu thuốc có thành phần hoạt chất khác nhau. Không được đặt tên thuốc khác nhau trong trường hợp thuốc có cùng công thức bào chế, cùng quy trình sản xuất của cùng một nhà sản xuất.














Bình luận